
Сеплайф ®Всё, что вам нужно знать об ионообменной хроматографии.
Введение в ионообменную хроматографию:
Ионообменная хроматография — это метод колоночной хроматографии, использующий разницу электростатических сил между обмениваемыми ионами на ионообменнике и различными ионами, разделяемыми в окружающей среде, и достигающий цели разделения посредством обменного равновесия. Ионообменная хроматография обладает преимуществами высокой чувствительности, воспроизводимости, хорошей селективности и высокой скорости анализа и в настоящее время является одним из наиболее часто используемых методов хроматографии.
В 1848 году Томпсон и др. открыли явление ионного обмена в процессе изучения обмена щелочных веществ в почве. В 1940-х годах появились полистироловые ионообменные смолы со стабильными характеристиками обмена. В 1950-х годах ионообменная хроматография вошла в область биохимии и была применена для анализа аминокислот. В настоящее время ионообменная хроматография по-прежнему является широко используемым методом хроматографии в области биохимии и широко применяется для разделения и очистки различных биохимических веществ, таких как аминокислоты, белки, сахара, вирусы и нуклеотиды.
Процесс ионного обмена:
Реакция между ионообменником и ионами или ионными соединениями в растворе в основном осуществляется путем ионного обмена. Происходящая ионообменная реакция обратима. Предполагая, что RA представляет собой катионообменник, катион A+, диссоциировавший в растворе, может вступать в обратимую реакцию обмена с катионом B+ в растворе, и формула реакции выглядит следующим образом:
RA + B+ → RB + A+
Реакция достигает равновесия с чрезвычайно высокой скоростью, и смещение равновесия подчиняется закону действия масс.
Селективность ионообменника может быть выражена константой равновесия K его реакции:
K = [RB][A+]/[RA][B+]
✔Если [A+] равно [B+] в реакционном растворе, то K=[RB]/[RA].
✔Если K>1, то есть [RB]>[RA], это означает, что сила связывания ионообменника с B+ больше, чем с A+;
✔Если K=1, то есть [RB]=[RA], это означает, что ионообменник обладает одинаковой силой связывания с A+ и B+;
✔Если K
✔Значение K — это параметр, отражающий силу связывания или селективность ионообменника по отношению к различным ионам, поэтому значение K называется коэффициентом селективности ионообменника для ионов A+ и B+.
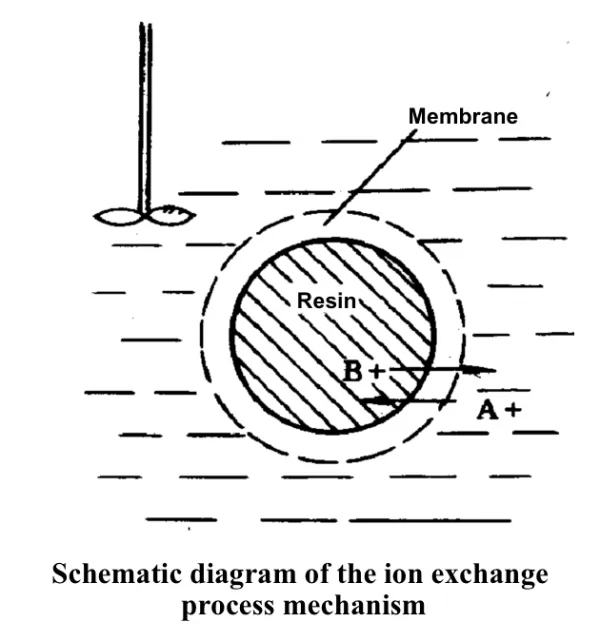
Механизм ионного обмена:
Ионы A+ диффундируют из раствора на поверхность смолы.
Ион А+ проникает в активный центр внутри смолы с поверхности смолы.
А+ вступает в реакцию метатезиса с РБ на активном центре.
Десорбированный ион B+ диффундирует из внутренней части смолы к ее поверхности.
Ионы B+ диффундируют с поверхности смолы в раствор.
Определяющим фактором скорости обмена является скорость диффузии, которая в различных системах разделения может регулироваться внутренней или внешней диффузией.
Факторы, влияющие на процесс ионного обмена:
✔Размер частиц: чем меньше, тем быстрее.
✔Степень сшивания: низкая степень сшивания, высокая скорость обмена.
✔Температура: чем выше температура, тем быстрее происходит процесс, это связано с увеличением коэффициента диффузии.
✔Валентность иона: чем выше валентность, тем медленнее скорость диффузии.
✔Размер иона: чем меньше, тем быстрее.
✔ Скорость перемешивания: в определенной степени, чем больше, тем быстрее.
✔Концентрация раствора: Когда скорость обмена контролируется диффузией, чем выше концентрация, тем быстрее скорость обмена.
Принцип ионного обмена:
Если выбрана катионообменная смола, положительно заряженное вещество обменивается на H+ и связывается со смолой. Если выбрана анионообменная смола, отрицательно заряженное вещество может обмениваться на OH- и связываться со смолой.
Существуют различия в степени прочности соединения веществ на смоле, и компоненты смеси могут элюироваться по одному путем выбора соответствующего элюента для достижения цели разделения и очистки.
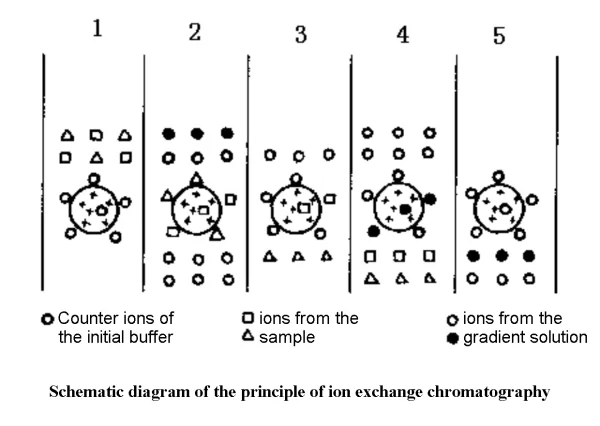
✔1. Этап уравновешивания: комбинация ионообменника и противоиона.
✔2. Этап адсорбции: обмен образца и противоионов.
✔3. Этап десорбции: сначала градиентный буферный раствор смывает слабо адсорбированные вещества, а затем — сильно адсорбированные вещества.
✔4. Этап регенерации: полная промывка исходным балансирующим раствором, который можно использовать повторно.
Смолы для ионообменной хроматографии:
Заряженные группы катионообменников имеют отрицательный заряд, а противоионы — положительный, что позволяет им осуществлять обменные реакции с катионами или положительно заряженными соединениями в растворе.
В зависимости от силы заряженной группы, ее можно разделить на три типа: сильнокислотный тип (группа с сульфоновой кислотой, R-SO3H), средне-сильнокислотный тип (содержащий фосфорнокислотную группу или группу фосфористой кислоты, R-PO3H2) и слабокислотный тип (с карбоксильной группой и фенольной смолой, R-COOH или R-бензольное кольцо-OH).
В процессе обмена в этих обменниках ионы водорода замещаются посторонними катионами, как показано в следующей формуле:
R-COOH+Na+=R-COONa++H+
Анионообменник образуется путем введения в матрицу групп четвертичного амина [-N(CH3)3], третичного амина [-N(CH3)2], вторичного амина [-NHCH3] и первичного амина [-NH2].
В зависимости от степени щелочности аминогрупп их можно разделить на три типа: сильноосновные (содержащие четвертичные аминогруппы), слабоосновные (содержащие третичные и вторичные аминогруппы) и среднеосновные (содержащие как сильноосновные, так и слабоосновные группы).
При обмене с ионами в растворе формула реакции выглядит следующим образом:
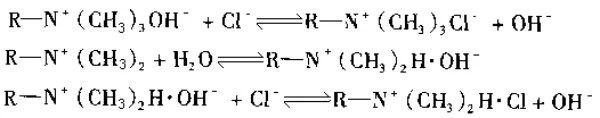
Для получения более подробной информации о конкретных типах ионообменных хроматографических смол следите за нашей следующей статьей об ионообменной хроматографии.














